La proteina della visione notturna: base per nuove terapie?
La proteina della visione notturna: base per nuove terapie?
I biologi del PSI hanno fatto luce su una vitale sostanza delle cellule a bastoncello della retina dell’occhio che aiuta a scrutare la penombra

Gli scienziati del PSI hanno fatto luce su un importante componente dell’occhio: una proteina nelle cellule a bastoncello della retina che ci aiuta a vedere in penombra. Come funziona la visione notturna?
Agendo come un canale ionico nella membrana cellulare, tale molecola biologica completa è responsabile della trasmissione del segnale ottico dall’occhio al cervello. Se un disordine genetico interrompe la funzione molecolare in una persona, questa diventerà cieca.
Gli scienziati hanno decifrato la struttura tridimensionale della proteina, preparando la strada a trattamenti medici innovativi.
Lo studio frutto del lavoro dell’Istituto Paul Scherrer è pubblicato sulla rivista scientifica “Nature Structural & Molecular Biology”.
Sede unica e il brand BIOS+ per gli istituti IRB, IOR ed EOC

(Foto: Markus Fischer/Istituto Paul Scherrer)
“Cellule tanto sensibili da rilevare anche un singolo fotone…”
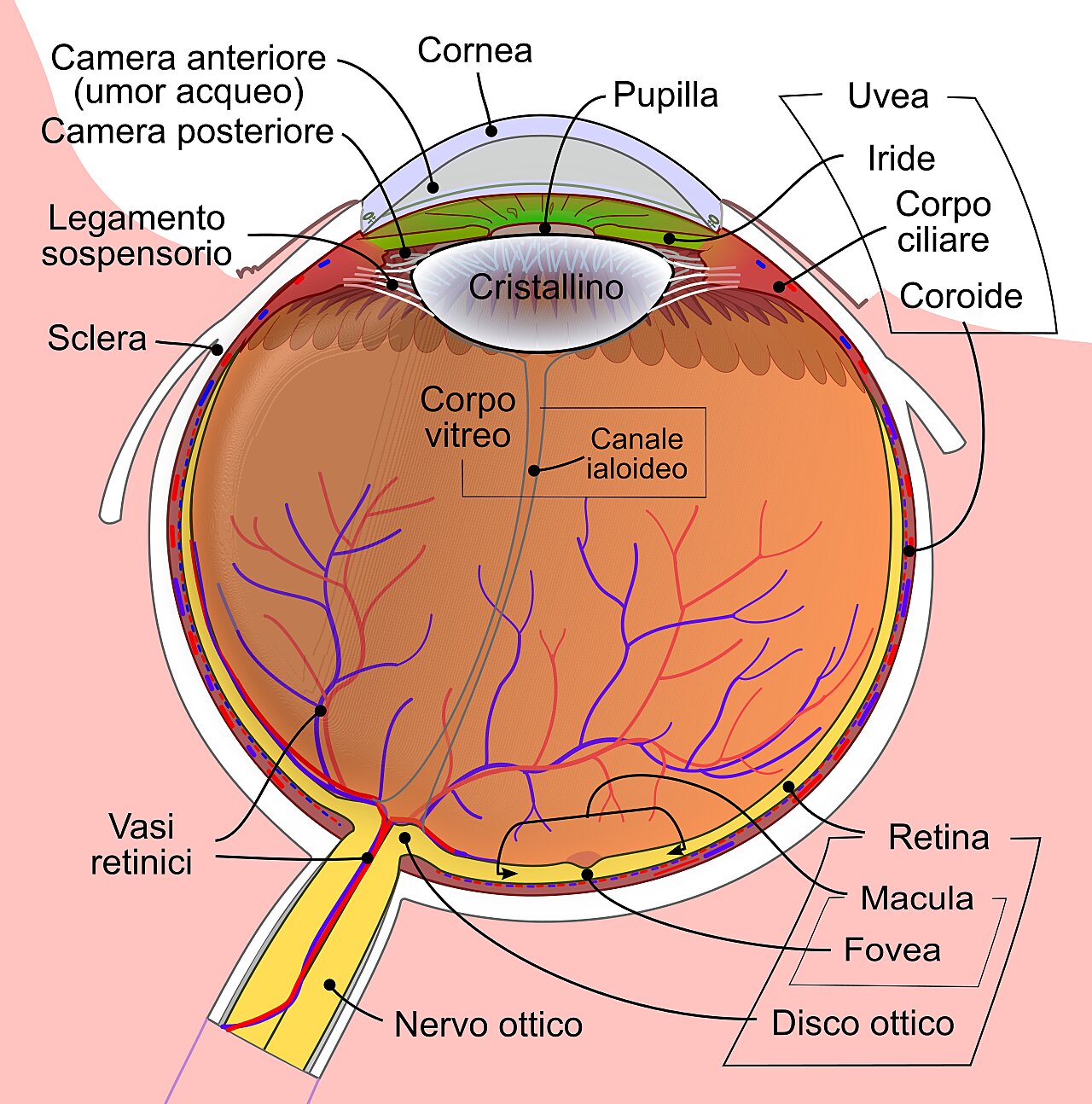
“È grazie alle cellule a bastoncello del nostro occhio che possiamo osservare le stelle nel cielo notturno”, spiega Jacopo Marino, biologo del Laboratorio di Ricerca Biomolecolare del PSI.
“Queste fotocellule sono così sensibili alla luce che possono rilevare anche un singolo fotone che ci raggiunge da una parte molto remota dell’universo, un’impresa davvero incredibile”.
La capacità del nostro cervello di tradurre questi fasci di luce in un’impressione visiva è in parte dovuta ai Canali Ionici a Nucleotidi Ciclici (CNG), la cui struttura tridimensionale è stata ora illuminata da un gruppo di ricerca dell’Istituto Paul Scherrer guidato da Jacopo Marino.
Il canale ionico agisce come una sorta di “guardiano”, che controlla se specifiche particelle sono ammesse all’interno della cellula recettore. È incorporato nel guscio ricco di proteine, la membrana cellulare, delle cellule a bastoncello.
I segreti di Omicron svelati a Losanna dal super microscopio
Vent’anni fa le ricerche di Gebhard Schertler e Benjamin Kaupp
Al buio, il canale ionico, e quindi il cancello della cellula, è completamente aperto. Ma quando la luce colpisce l’occhio, innesca una cascata di processi nelle cellule del bastoncello.
Questo alla fine causa la chiusura della porta, con il risultato che le particelle caricate positivamente, come gli ioni di calcio, non possono più entrare nella cellula.
Questo segnale elettrochimico continua attraverso le cellule nervose nella corteccia visiva del cervello, dove viene creata un’impressione visiva, come un lampo di luce.
“L’idea di comprendere la struttura di questo canale risale a quasi venti anni fa, quando Gebhard Schertler e Benjamin Kaupp già collaboravano su questo argomento”, commenta Jacopo Marino. Entrambi sono co-autori del nuovo studio made-in-Switzerland, in tema di visione notturna?
In Svizzera la digitalizzazione prende piede in agricoltura

Due anni per estrarre la molecola dal canale oculare dei bovini
La dottoranda Diane Barret ha dovuto prima estrarre la proteina del canale dagli occhi delle mucche fornite da un macello, un processo complicato e arduo.
“Questo è stato un compito molto impegnativo, poiché la proteina è estremamente sensibile e si decompone molto rapidamente. Inoltre, è disponibile soltanto in piccole quantità nel materiale di partenza”, spiega la Barret. Ci sono voluti ben due anni per ottenere abbastanza proteine con cui lavorare.
“Eravamo entrambi semplicemente troppo testardi per rinunciare”, aggiunge Jacopo Marino, ridendo. “Ma alla fine quella testardaggine ha pagato…”.
Problemi di pressione? Tutti li abbiamo, ma poche regole…

“Abbiamo studiato la sostanza nativa com’è davvero nell’occhio”
Gli scienziati hanno poi usato la crio-microscopia elettronica per rivelare la struttura tridimensionale del canale ionico.
“A differenza degli studi precedenti sulla struttura del canale ionico, abbiamo studiato la proteina nativa come esiste, com’è davvero nell’occhio. Siamo quindi molto più vicini alle condizioni reali che esistono negli esseri viventi”, dice Diane Barret, esperta della visione notturna.
Uno dei motivi per cui una comprensione più chiara della struttura naturale della proteina del canale è importante è quello di far progredire lo sviluppo di trattamenti per i disturbi genetici per i quali non esiste una cura conosciuta, come la retinite pigmentosa.
Che cos’è la Sindrome Metabolica? E come si può prevenire?

(Foto: Markus Fischer/Istituto Paul Scherrer)
Un’inedita chiave per combattere la cecità da retinite pigmentosa
Con questa malattia, i fotorecettori muoiono gradualmente, lasciando le persone cieche. Una possibile causa è che il corpo non è in grado di produrre correttamente la proteina del canale CNG a causa di un difetto genetico.
Di conseguenza, il canale ionico non si chiude completamente quando la luce colpisce l’occhio, disturbando l’equilibrio elettrochimico della cellula e causando la morte delle cellule.
“Se potessimo trovare delle molecole che influenzano la proteina in modo tale che il canale si chiuda completamente, potremmo impedire alle cellule di morire, e quindi impedire alle persone di diventare cieche”, spiega Jacopo Marino.
Ora che i ricercatori hanno identificato la struttura precisa della proteina, sono in grado di cercare specificamente tali molecole e combattere la cecità da retinite pigmentosa.
Si chiama Parabulina il nuovo “castigamatti” dei parassiti
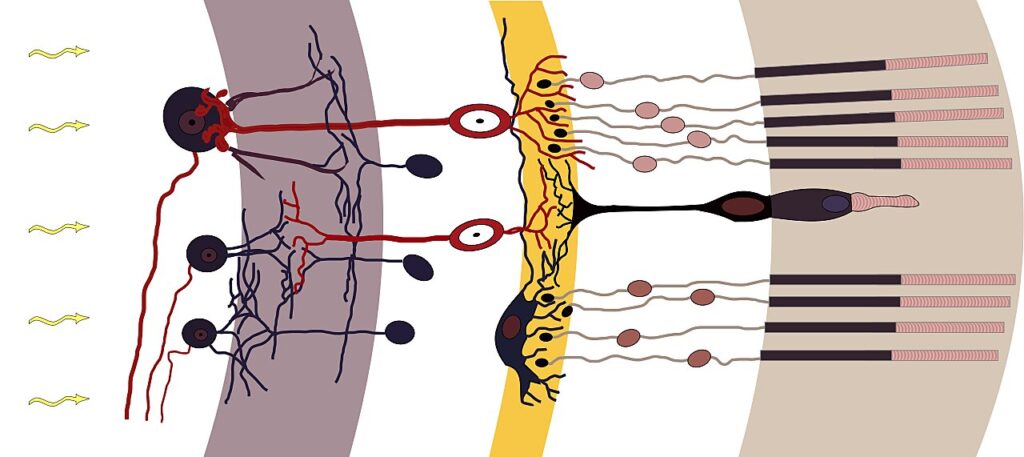
Sorpresa: la barriera sporgente formata da un singolo aminoacido
La proteina comprende quattro parti: tre lotti di subunità A e un lotto di subunità B. Un canale ionico correttamente funzionante è possibile soltanto in questa combinazione.
Nel loro studio, gli scienziati del PSI mostrano perché la subunità B sembra giocare un ruolo così importante: un braccio laterale della proteina, segnatamente un singolo aminoacido, sporge dal resto della proteina, come una barriera attraverso un passaggio.
Questo restringe il passaggio nel canale al punto in cui nessun ione può passare.
“Nessuno se lo aspettava, è stata una sorpresa totale”, dice Diane Barret. Altri luoghi stretti esistono già nella subunità A, come i gateway principali, che prima si pensava fossero gli unici.
È interessante notare che la barriera aggiuntiva si trova non soltanto nella proteina dell’occhio della mucca, ma sembra applicarsi a tutti i tipi di animali, come hanno dimostrato gli scienziati.
Che si tratti di coccodrilli, aquile o esseri umani, tutte le creature viventi con un canale ionico nel loro occhio hanno lo stesso aminoacido sporgente in questa posizione nella proteina.
Essendosi conservato così costantemente durante l’evoluzione, deve essere essenziale per il funzionamento del canale. E per la visione notturna.
Depressione e alimentazione: qual è il nesso inestricabile?

(Foto: Markus Fischer/Istituto Paul Scherrer)
Potresti essere interessato anche a:
Austria, Germania e Svizzera per ferrovie cargo “più innovative”
I Ministri DACH Leonore Gewessler, Volker Wissing e Albert Rösti: un elemento chiave l’introduzione dell’Accoppiamento Automatico Digitale
Persuasione o manipolazione? Genesi e impatto storico delle PR
Ecco come le Relazioni Pubbliche, dal dialogo sofistico dell'antica Grecia all’attuale era digitale, continuano a offrire una innovazione continua
I giovani e le crypto: come fare a saperne di più del Bitcoin…
Avvicinare i ragazzi a valute digitali e Blockchain può essere un'impresa entusiasmante, data la loro affinità con la tecnologia e l'innovazione
“Il paziente al centro”: un grande auspicio e un incontro al Senato
Il tema dell’importanza dell’innovazione nei dispositivi medici per la sanità europea sarà sviscerato il 15 maggio a Roma da esperti e politici
by Alberto NicoliniEditore di distrettobiomedicale.it, BioMed News e Radio Pico




