Sviluppo di nuovi farmaci, librerie potenziate grazie alla chimica
Dai laboratori dell'EPFL un metodo inedito per produrre più velocemente i composti da cui possono nascere i medicinali del futuro

I ricercatori dell’Ecole Polytechnique Fédérale de Lausanne (EPFL) hanno sviluppato un nuovo metodo che permette di ottenere e identificare decine di migliaia di composti macrociclici in appena mezza giornata.
Si tratta di un’innovazione cruciale soprattutto per la ricerca in ambito farmacologico: i macrocicli, infatti, sono molecole molto usate per lo sviluppo di nuovi farmaci capaci di “colpire” bersagli considerati difficili, come per esempio alcuni tumori.
Le librerie chimiche, i “database” di molecole utilizzati per individuare i possibili candidati a diventare farmaci, potranno così contare su collezioni di composti molto più ricche, realizzate in modo rapido e sostenibile.
Le sorprese della chimica: così i rifiuti in plastica diventano sapone
Un’innovativa tecnologia quantistica tutta basata sul carbonio

Le librerie chimiche per lo sviluppo di medicinali davvero innovativi
Agli albori della farmacologia, i farmaci erano sintetizzati a partire dai derivati di alcune piante medicinali, oppure scoperti in maniera più o meno fortuita nell’ambito della ricerca scientifica. La vera svolta per la disciplina, molto florida già alla fine dell’Ottocento, è arrivata negli anni Sessanta del secolo scorso, quando le importanti scoperte in ambito di biochimica hanno permesso di iniziare a sviluppare nuovi farmaci a partire da una progettazione più razionale.
Grazie alla sempre più dettagliata comprensione del funzionamento dei recettori, la ricerca di nuovi principi attivi divenne un’attività più metodica e razionale, che poteva sfruttare il “reverse engineering” per sviluppare nuovi composti in grado di legarsi a questa o quella molecola.
Oggi moltissimi farmaci sono progettati secondo il modello target-based drug discovery, cioè a partire dal bersaglio su cui si vuole intervenire: buona parte della ricerca è quindi rivolta a individuare nuove molecole capaci di agire sui target e produrre gli effetti terapeutici desiderati.
Uno dei metodi più utilizzati per identificare nuovi composti e principi attivi è quello degli screening ad alta intensità (High-throughput Screening), che permettono di testare in poco tempo l’azione di un gran numero di composti chimici su una determinata proteina bersaglio.
Le librerie chimiche svolgono in tal senso una funzione di primaria importanza: possiamo immaginarle come dei database che permettono conservare e catalogare una gran quantità di sostanze chimiche, potenziali candidati farmaci a disposizione degli scienziati impegnati nella ricerca di nuove cure.
La natura ti fa… giovane! Così il verde rallenta l’invecchiamento
L’innovazione chiave del distretto biomedicale di Mirandola

Una classe di molecole molto promettente per i farmaci del futuro
Oggi le case farmaceutiche hanno accesso a librerie chimiche in cui sono raccolti e catalogati anche uno o due milioni di composti “micromolecolari”. In molti casi, però, le tecniche di screening tradizionali non consentono di identificare i possibili candidati a farmaco perché le librerie non contengono composti che si legano in maniera sufficientemente forte al bersaglio.
Una soluzione in tal senso è costituita dai macrocicli, una classe di molecole emergenti in grado di legarsi in maniera efficace a bersagli particolarmente difficili da agganciare, come alcune proteine.
Il problema è che librerie di macrocicli attualmente contengono al massimo 10.000 composti, cosa che limita di molto le possibilità di trovare il giusto candidato da scatenare contro una certa malattia target.
La scoperta da cui potrebbe derivare un’intera generazione di nuovi farmaci è avvenuta lo scorso anno nei laboratori dell’Ecole Polytechnique Fédérale de Lausanne: un gruppo di chimici ha messo a punto un nuovo metodo per generare e identificare in modo rapido e sostenibile migliaia di composti macrociclici, alimentando in maniera significativa le librerie disponibili.
La scoperta, che apre nuove possibilità per la cura di gravi malattie come i tumori, si deve al team del professor Christian Heinis della School of Basic Sciences dell’EFPL. I risultati della ricerca, nata dalla collaborazione con le Università di Padova e di Venezia, sono stati pubblicati a luglio 2022 sulla rivista internazionale “Nature Communications”.
Che cos’hanno in comune molte eccellenze alimentari e l’Eparina?
MSD, in Olanda il comparto farmaceutico si tinge di verde
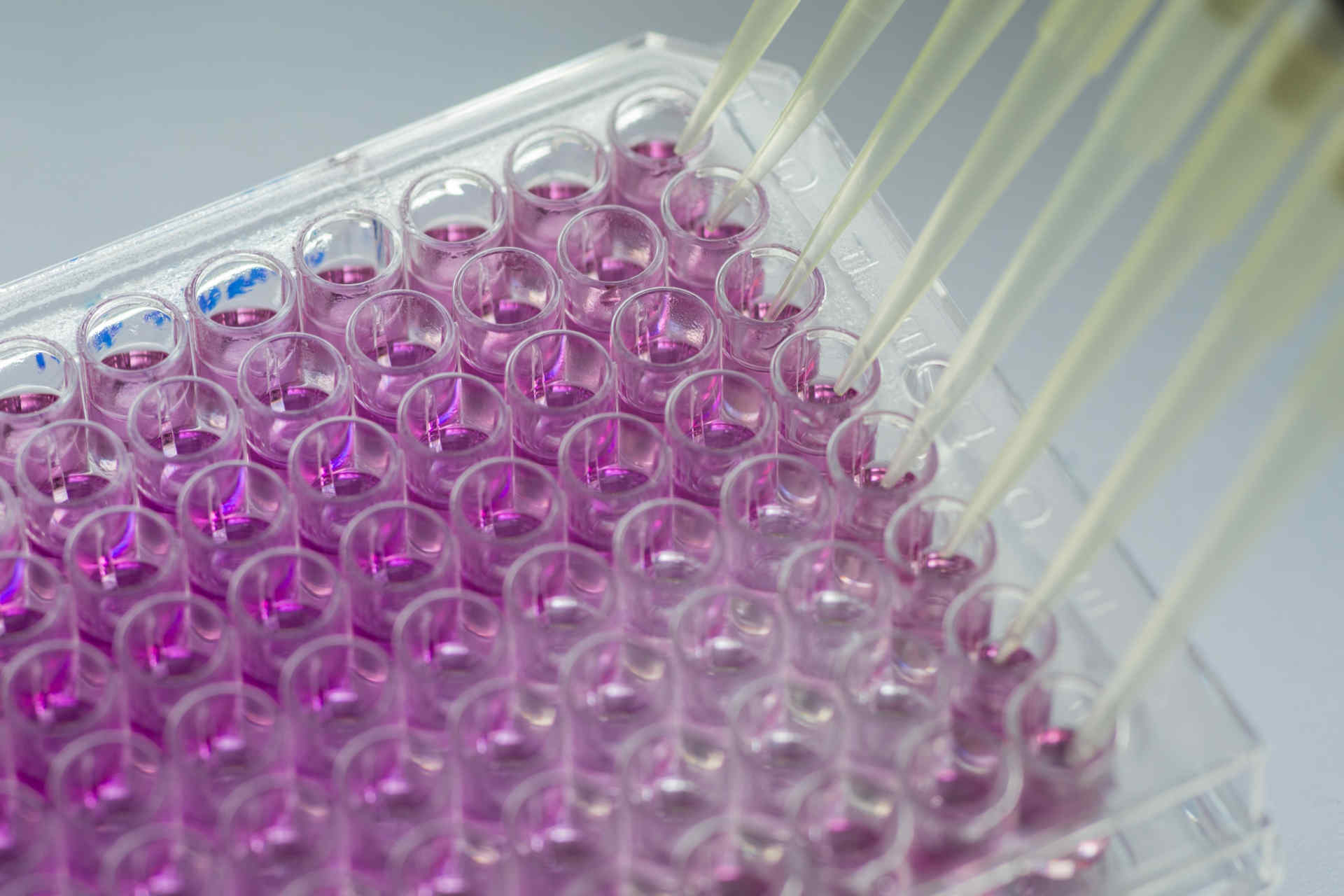
Produzione “accelerata” di macrocicli in un minuscolo spazio vitale
Nella maggior parte dei programmi di ricerca volti alla scoperta di nuovi farmaci, spiega l’Università Ca’ Foscari, “un gran numero di composti chimici strutturalmente diversi raccolti nel corso di molti anni viene testato contro una determinata proteina bersaglio”.
Questi esperimenti solitamente sono eseguiti in piastre da centinaia di micropozzetti, ognuno contenente un composto da analizzare. Come è facile intuire, si tratta di “una procedura che richiede molti giorni, costi ingenti e consumi elevati di sostanze chimiche”, e che non sempre conduce all’individuazione di molecole promettenti.
Quello sviluppato nei laboratori dell’EPFL è un nuovo metodo che permette di sintetizzare grandi collezioni di composti in modo estremamente rapido, grazie alla miniaturizzazione dei processi e all’uso delle onde acustiche.
Lavorando su volumi estremamente piccoli, nell’ordine dei nanolitri, e mescolando i reagenti ad alte velocità grazie all’utilizzo della tecnologia di Espulsione Acustica delle Goccioline (ADE), è stato possibile ottenere decine di migliaia di composti diversi in appena mezza giornata.
“Il nostro approccio è basato sulla combinazione di un gran numero di scaffold macrociclici diversi ‘m’ con una miriade di frammenti chimici ‘n’ per generare diversi composti macrociclici ‘mxn’”, spiega il Professor Christian Heinis.
“Per esempio”, continua il professore, “abbiamo generato una libreria di 19.968 macrocicli facendo reagire 192 scaffold macrociclici con 104 frammenti di acidi carbossilici”.
Rimpicciolire i processi fino alla scala picomolare, lavorando in piccolissime gocce, ha permesso di velocizzare il processo e renderlo più sostenibile.
Si chiama Parabulina il nuovo “castigamatti” dei parassiti
Una dieta innovativa (e ragionata) per battere il colesterolo
Le molecole ai raggi X e le prospettive per lo sviluppo di nuove cure
Gli scienziati del team del dottor Heinis hanno sperimentato le reazioni in microscopici volumi (40 nanolitri) e trasferito i reagenti usando le onde acustiche.
Sevan Habeshian, il dottorando alla guida del progetto, ha testato il nuovo metodo applicandolo allo sviluppo di inibitori nanomolari della trombina (target di farmaci contro le malattie cardiache) e dell’interazione proteina-proteina MDM2:p53, un bersaglio delle terapie antitumorali.
Grazie alla collaborazione con l’Università di Padova e l’Università Ca’ Foscari di Venezia, i ricercatori hanno potuto indagare la struttura tridimensionale a raggi X dell’inibitore della trombina legato alla proteina bersaglio.
“La risoluzione della struttura tridimensionale ai raggi X ha rivelato che entrambe le componenti, i gruppi chimici introdotti ma anche lo scheletro del macrociclo stesso, contribuiscono in modo fondamentale al legame”, spiega la professoressa Laura Cendron, docente presso il Dipartimento di Biologia dell’Università di Padova.
I composti macrociclici ottenuti col nuovo metodo si confermano quindi efficaci nel legarsi a proteine difficili, e le nuove librerie arricchite potrebbero contenere la cura per malattie che sono ancora problematiche da trattare farmacologicamente.
“Stiamo applicando questo approccio allo sviluppo di composti macrociclici diretti a una varietà di target problematici”, per cui è difficile sviluppare nuovi farmaci a partire dalle classiche micromolecole, spiega ancora Heinis.
“Data la dimensione contenuta e la piccola superficie polare, i composti macrociclici hanno buone possibilità di attraversare le membrane cellulari”, continua il docente svizzero, “il che significa che possono essere usati per sviluppare farmaci per bersagli intracellulari o anche medicinali da assumere per via orale”.
Canapa in vendita: inedita sperimentazione a Basilea Città
Tutto ciò che di “innovativo” c’è da sapere sulla Vitamina D

Potresti essere interessato anche a:
“Ossigeno oscuro”: l’inedita scoperta sul fondo dell’Oceano
I noduli polimetallici sui fondali del Pacifico producono l'elemento "O": l'eclatante rivelazione solleva ulteriori domande sul deep sea mining
Stati Uniti: Grana Padano protagonista della ristorazione
Il Consorzio di Tutela vola a San Antonio per la prima tappa di una campagna che sensibilizza i consumatori sul tema dell’Italian Sounding
Deep Sea Mining, la corsa all’oro che minaccia le balene
L'allarme degli scienziati: se l’ISA darà il via libera all’estrazione di minerali sui fondali marini ci saranno conseguenze catastrofiche...
Tutta l’innovazione dell’approdo del Gruppo Chery in Europa
Il 4 luglio i brand cinesi Omoda e Jaecoo hanno fatto il loro debutto a Milano e sul nostro mercato con auto sostenibili e al passo dei tempi




